
C’est la technologie de stockage électrochimique qui émerge tout juste, mais qui a le vent en poupe : la batterie sodium-ion. Certains la voient remplacer à terme la batterie lithium-ion. Nous n’en sommes pas là, et de loin. Nous pouvons toutefois nous intéresser à leur fonctionnement, et l’origine de toutes les promesses qui entourent son apparition.
Les batteries sodium-ion sont une alternative émergente aux batteries lithium-ion, pour le stockage d’électricité. Elles présentent en effet des caractéristiques redoutables vis-à-vis de ces dernières. La première tient lieu de l’abondance de la ressource : le sodium est plus de mille fois plus abondant que le lithium dans la croûte terrestre (2,36 % par rapport à 0,002 %, d’après le CRC Handbook of Physics). Par ailleurs, il est disponible partout, facilement accessible, notamment dans l’eau de mer ; le simple sel marin en contient en effet une grande part.
Cela fait de cette technologie un atout de choix pour envisager une réduction du prix des batteries, une moindre dépendance à des importations restreintes d’un point de vue géographique, ainsi qu’un moindre impact environnemental induit par l’extraction des matières premières. Il faut toutefois tempérer ce point par le fait que les électrodes peuvent contenir d’autres substances, potentiellement rares, comme le vanadium.
À lire aussiVoici la plus grande batterie sodium-ion du mondeLes batteries sodium-ion ont en revanche une moindre densité d’énergie ; cela peut s’avérer problématique pour les applications mobiles, mais est de moindre importance pour les batteries stationnaires. Leur durée de vie en termes de nombre de cycles est aujourd’hui moindre, également. En revanche, les batteries sodium-ion seraient plus sûres, vis-à-vis du risque d’incendie, tout en supportant une plus grande puissance de charge et de décharge, permettant des cycles plus rapides.
Notons que ces appréciations restent qualitatives, et ne font que souligner des tendances générales ; en effet, les données chiffrées des performances varient dans une large part, elles sont généralement basées sur des prototypes ou des têtes de série, et elles évoluent vite.
Parmi les fabricants de batteries sodium-ion, aujourd’hui de plus en plus nombreux, citons au passage la société française Tiamat, fondée à partir de travaux de recherche du CNRS, et qui a pour projet d’implanter une gigafactory du côté d’Amiens. Tiamat avait fait parler d’elle fin 2023 lorsqu’il avait été annoncé par Leroy Merlin la commercialisation de la première visseuse sans fil à batterie sodium.

Une batterie sodium-ion est un ensemble de cellules encloses dans une enveloppe de protection. Chaque cellule contient un accumulateur, qui est le composant même où est stockée l’énergie. Un accumulateur est constitué d’une électrode positive et d’une électrode négative entre lesquelles est intercalé un séparateur, dont la fonction est d’éviter les courts-circuits entre les deux électrodes. L’ensemble est immergé dans un électrolyte.
Un accumulateur sodium-ion stocke l’énergie sous forme chimique, ce qui signifie que la charge et la décharge de la batterie vont mettre en jeu des réactions chimiques. De ce fait, un accumulateur sodium-ion est un moyen de stockage appelé « accumulateur électrochimique », une grande famille qui regroupe la grande majorité des batteries de la vie quotidienne.
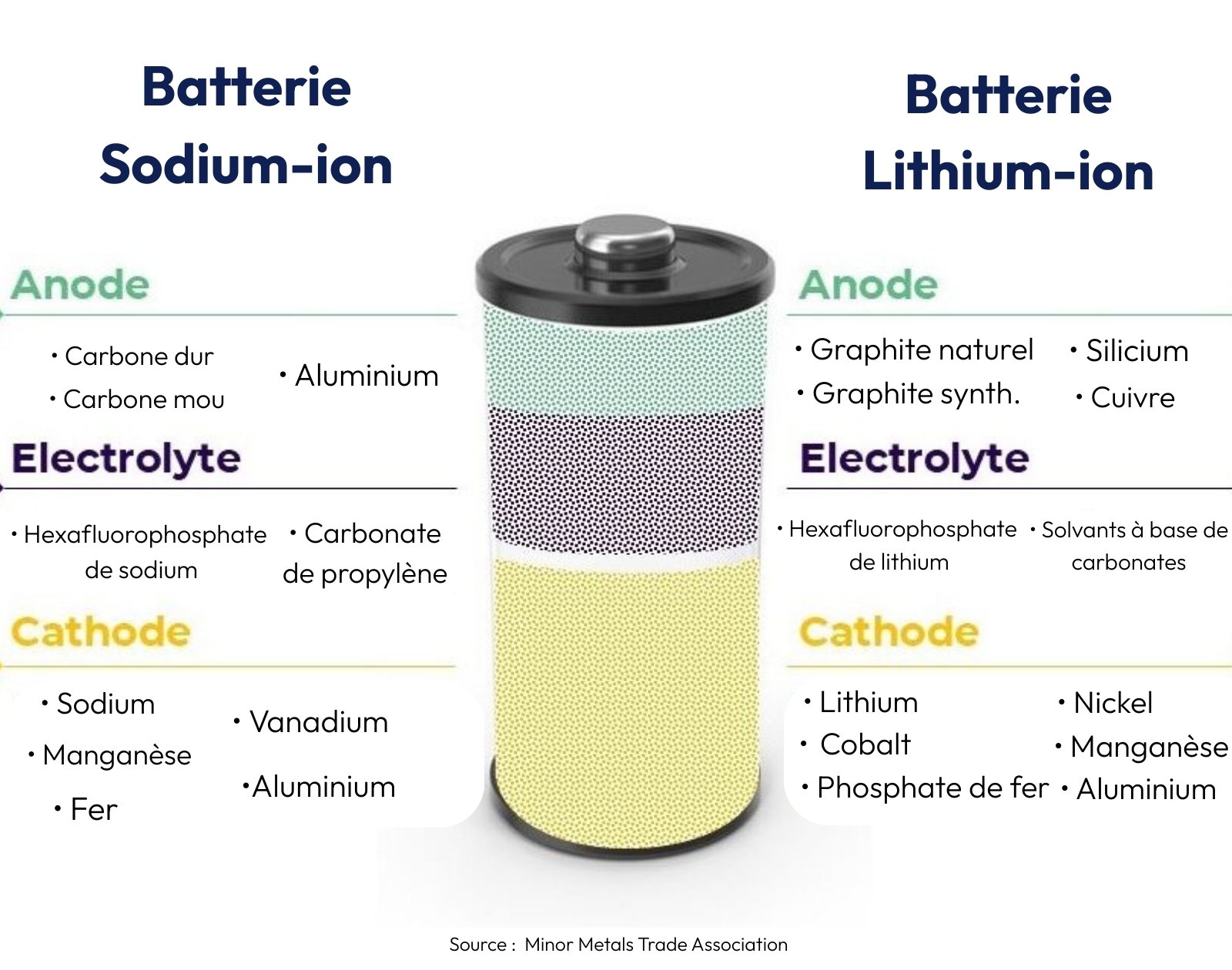
L’accumulateur sodium est basé sur l’échange réversible de l’ion sodium Na+ entre une électrode positive et une électrode négative. En effet, les matériaux de l’anode et de la cathode sont tous les deux des substrats, qui peuvent contenir dans leur structure atomique des atomes de sodium, et ce sodium va circuler entre les deux électrodes au travers de l’électrolyte. Il s’agit d’un principe de fonctionnement tout à fait similaire aux batteries lithium-ion (Li-ion), quant à elles basées sur l’échange réversible de l’ion lithium Li+.
Lors de la décharge, l’accumulateur est une source d’énergie, les réactions chimiques sont donc spontanées. Pour qu’elles se produisent, il faut fermer le circuit électrique, et permettre la circulation des charges électriques. À l’extérieur de la batterie, l’électrode positive est connectée avec l’électrode négative par un circuit électrique extérieur, contenant la charge que l’on cherche à alimenter en électricité. À l’intérieur de la batterie, c’est la circulation des ions sodium qui va transmettre le courant à l’intérieur de la batterie. Lors de la décharge, les ions Na+ se désintercalent du substrat de l’anode et migrent au travers l’électrolyte vers la cathode, tandis que des électrons circulent de l’anode vers la cathode par le circuit externe.
Au cours de la charge, il se produit la réaction inverse. Une tension est appliquée aux bornes de l’accumulateur. Sous l’effet de cette tension, les ions Na+ vont se désintercaler du substrat de la cathode et migrer au travers l’électrolyte pour s’intercaler dans le matériau de l’anode, tandis que des électrons circulent de la cathode vers l’anode par le circuit externe.
À lire aussiComment fonctionne une batterie sodium-ion ?Les matériaux qui constituent les électrodes peuvent être d’une nature très différente, au même titre que les batteries Li-ion – ces dernières comptent dans leurs rangs une grande variété de compositions, définies par leurs sigles : LCO, NMC, LFP, etc. Pour les accumulateurs sodium-ion, en ce qui concerne l’électrode positive, les recherches se concentrent notamment les phosphates, et notamment une variante particulière, appelée NaSICON (pour Sodium super ionic conductor). Cette dernière est constituée d’un mélange de sodium, de vanadium et de phosphates. Ils présentent une grande variété de phases cristallines, offrant des sites variés pour accueillir l’ion sodium. C’est une variante de ce matériau qui a été utilisée par Tiamat, plus précisément le Na3V2(PO4)2F3 ; NVPF, de son petit nom.
En ce qui concerne l’électrode négative, le carbone est très utilisé, comme pour les batteries Li-ion ; ce carbone peut se trouver sous toutes ses formes : graphite, graphène, carbone amorphe… Mais d’autres matériaux font aussi l’objet de développements : des oxydes, des sulfates, des phosphates, des alliages métalliques… en pratique les options sont innombrables. Pour continuer sur notre exemple, Tiamat utilise des électrodes en carbone amorphe dit « dur » (en anglais « hard carbon », ou HC).
La suite de votre contenu après cette annonce
Notre Newsletter
Ne ratez plus les dernières actualités énergetiques
S'inscrire gratuitement